Последнее десятилетие ознаменовалось таким развитием общей химии (напомним лишь такие открытия, как установление порядковых чисел элементов, установление генетической связи радиоэлементов, нахождение изотопов), что наряду с этим успехи в специальной области химии углерода, успехи, которые в течение предыдущих 10 лет налагали свою печать на все развитие химии, несомненно отходят на второй план.
Как и во всех экспериментальных естественных науках, и в современной химии углерода можно отметить два строго отличных направления работы: или исходят из теоретической предпосылки, которую стараются экспериментально доказать, благодаря чему часто создаются новые вещества, видоизменяются существующие методы работы и создаются новые, или, благодаря большой наблюдательности, удается установить опытным путем новые явления и, углубляясь в эти наблюдения, иногда находят новую возможность разрешения теоретической проблемы. Так, в 1865 г. Байер ввел важный метод перегонки с помощью цинковой пыли в то время, когда он стремился приготовить вещество C8H7N, которое принималось им на основании теоретической предпосылки за основную субстанцию индиго, для которого он уже заранее придумал название "индол". Так, с другой стороны, открытый Эмилем Фишером фенилгидразин, благодаря своей высокой реакционной способности, помог раскрыть и изучить такую важную главу органической химии, как сахара, а вместе с тем развить и стереохимические теории.
Мы в настоящей заметке попытаемся отметить лишь некоторые экспериментальные достижения органической химии.
Исследование органического вещества распадается на три части: при помощи анализа мы определяем его состав, при помощи молекулярного веса — величину его частичек, при помощи разнообразнейших превращений мы устанавливаем строение вещества из элементов. Особенных успехов достигла химия в последнем случае, но и в первых двух совершилась большая эволюция, которую можно кратко назвать "микронизациею операций". Органический микроанализ, разработкой которого мы обязаны, главным образом, австрийскому химику Pregl’ю, от обычного органического анализа отличается лишь участием меньших количеств веществ (в мгр.) и уменьшением, соответственно этому, всей аппаратуры. Микровесы позволяют производить взвешивание с точностью до 0.001 мгр. Главная ценность микроанализа заключается в экономии исходного материала, и целый ряд исследований, например, нуклеиновых кислот (работы Wieland’a, Levene) — был бы немыслим без применения микроанализа. Немного менее, чем микроанализ, применяется микроопределение молекулярных весов. Хотя обыкновенные эбуллиоскопические и криоскопические методы можно при соблюдении известных условий приспособить к определениям маленьких количеств, гораздо большее будущее имеет поразительно простой метод, которым мы обязаны Barger'y (Лондон). Он основан на простом принципе: растворитель из разбавленного раствора стремится перейти в более концентрированный, чтобы уравнять концентрацию. Представим себе, что мы имеем в капилляре две капли, диаметр которых мы наблюдаем под микроскопом с помощью соответственно устроенной скалы. Если растворы обоих капель эквимолекулярны, то ничего не изменится, в противном случае одна из капель удлинится. Таким образом, чтобы определить молекулярную концентрацию неизвестного раствора и отсюда обычным путем молекулярный вес, нужно только капельки исследуемого раствора привести во многих капиллярах в соприкосновение с капельками стандартных растворов соответственным образом измененной молекулярной концентрации, пока не будет найдена та концентрация, при которой капельки останутся без изменения. Некоторое усовершенствование этого простого метода недавно было произведено в Вюрцбургской лаборатории.
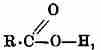
Точно также в области применения физических факторов для химических целей мы можем констатировать ряд успехов в направлении "микронизации". Как известно, оптические свойства давно играли большую роль при исследовании органических веществ и определении строения органической молекулы, но пределом этих исследований служила чувствительность нашего глаза, воспринимающего только маленькую часть световой волны — 0,04—0,08 µ, открытие и применение ультра-фиолетовых и рентгеновых лучей в области органических исследований вскоре позволили расширить эти пределы. Источник света, богатый ультра-фиолетовыми лучами, помещается перед щелью спектрального аппарата, пучек лучей разлагается призмой, проходит через вещество, абсорбционная способность которого определяется, и падает на фотографическую пластинку, позволяющую после проявления весьма точно установить происшедшую абсорбцию. Пионером в этой области является Miller (1862) и Hartley (1879); V. Henri значительно усовершенствовал в последнее время этот метод. Многочисленные исследования, произведенные в новейшее время на родине Hartley’а в Англии, а, главным образом, в Лейпциге Hantzsch’ем и его школой, показали возможность широкого применения его, в особенности для тех веществ, которые для нашего глаза кажутся бесцветными или слабо окрашенными, каковыми являются сравнительно простые органические вещества. Чем сложнее молекулы, тем больше абсорбция перемещается по направлению коротких волн и выступают красный, зеленый, синий и, наконец, фиолетовый цвета, совершенно отсутствующие при более просто построенных органических веществах. К таким бесцветным веществам, но довольно сильно абсорбирующим в ультра-фиолетовом цвете, принадлежит бензол, основа наших смоляных красок. Большие услуги исследование ультра-фиолетовой абсорбции оказало при таутомерии. Лишь на одном примере мы покажем те поразительные результаты, к которым может привести применение этого метода в случаях, казалось бы, совершенно ясных. Если мы имеем дело с любой органической карбоновой кислотой R·CO2H, то мы ей приписываем структурную формулу:

ее солям формулу:
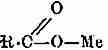
и ее эфирам формулу:
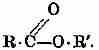
Единственная разница, известная нам со времени основания и развития электролитической теории диссоциации, состоит в том, что в кислотах и солях связь между О и Н или Me в определенных растворах, прежде всего в воде, более слабая, что же касается общих условий связи, в особенности комплексной
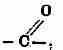
то она не изменяется. Так как степень диссоциации или ассоциации не влияет на абсорбцию и почти не влияют водородный атом, оптически индиферентный атом щелочных или щелочно-земельных металлов и наконец, насыщенный алкильный остаток, то надо было предположить, что между абсорбцией кислот, солей и эфиров существует лишь минимальное различие. Оптические исследования показывают, однако, совершенно противоположное:
все эфиры абсорбируют между собой одинаково, независимо от величины R'
все соли (в особенности щелочные и щелочно-земельные) отличаются одинаковой взаимной поглощательной способностью, но отличною от эфиров, при первых слабее, чем при последних;
величина абсорбции кислот колеблется между солями и эфирами.
Для эфиров установлено, что они имеют выше приведенную формулу. Если соли и кислоты различно абсорбируют, то на основании данных спектроскопии их молекулы должны отличаться своим строением, и так как диссоциация сама не дает объяснения этого, то единственная возможность остается та, что водород и металлы не находятся, как алкильные остатки около одного кислородного атома, а что они находятся в сфере притяжения обоих кислородных атомов:
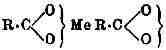
Эта формулировка не вкладывается в наши обычные валентные формы, но находит место в схеме теоретических представлений А. Вернера. При солях, очевидно, существует своеобразное строение молекул, кислоты со средней абсорбцией примыкают частью к солям, частью к эфирам:
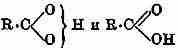
это тем более вероятно, что, если водород с одной стороны кажется аналогом щелочных металлов, то с другой стороны он является конечным членом в гомологическом ряду алкильных остатков.
Несомненно, что изучение тех же процессов в области инфра-красных лучей в будущем окажется чрезвычайно важным для химии углерода. В недавнее время удалось применить Рентгеновские лучи в органохимическом исследовании. Herzog со своими сотрудниками в Kaiser Wilhelm Institut, пользуясь открытиями Laue, Friedrich’a, Knipping’a, обоих Bragg’ов, Debye и Scherrer’a, приступил к исследованию высоко-молекулярных органических веществ, главным образом, целлулозы, крахмала, гликогена, искусственного шелка, шерсти, человеческого волоса. В результате этих исследований оказалось, что часть этих молекулярных веществ, как и предполагалось, несомненно аморфны, например, шерсть, волос, гликоген, с другой стороны, шелк, целлулоза и крахмал оказываются кристаллическими. Целлулоза, как известно, при гидролизе, точно так же, как и крахмал, распадается на молекулы виноградного сахара, но если гидролиз проводить очень осторожно, то большею частью удается получить (смотря по условиям работы от 35 до 60%) две молекулы виноградного сахара и один из многих известных ди-сахаридов, так называемую, целлобиозу.
Измерение состава элементарного тела целлулозной молекулы показало, что она состоит из 4-х остатков виноградного сахара и так как кристаллы целлулозы принадлёжат к гемиморфной группе моноклинической системы, то на основании кристаллографической симметрии, следует, что каждое элементарное тело должно состоять из двух двойных сахаров, т. е., из остатков целлобиозы, и вся целлулоза должна быть составлена из целлобиоз таким образом, что комплексы двух между собой соединенных остатков целлобиозы повторяются n раз в молекуле; прежняя схематическая структурная формула целлулозы (где z означает остаток виноградного сахара
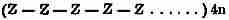
заменяется формулою:
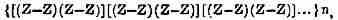
и рентгено-оптике принадлежит окончательное решение вопроса о строении этой большой молекулы.
Мы уже указывали на некоторые успехи, достигнутые при определении строения органических веществ при переходе от видимого света к ультра-фнолотовому. Уже давно известно, что световая энергия используется для химических превращений и что действие лучей почти без исключения увеличивается с уменьшением длины волны, отсюда естественна мысль применить ультра-фиолетовые лучи к химическим превращениям в области органической химии. До сих пор таких исследований произведено мало, но им несомненно принадлежит большое будущее в химии углеродов, — укажем здесь лишь на два факта, которыми мы обязаны Ростокскому органику Strömer’y и его ученикам. Во-первых, как известно, соединения с двойной связью могут существовать в гемиморфных изомерных модификациях, из которых одна соответствует более прочному, а другая — более лабильному молекулярному строению, как, например, две коричные кислоты, более высоко плавящиеся — более прочная и легко изолируемая. Исследование этих изомеров составило задачу трудных, остроумных и тщательных многолетних исследований. Было известно, что под действием света лабильная гемиморфная изомерия может перейти в стабильную. Strömer показал, что при достаточном количестве ультра-фиолетового цвета возможен и обратный переход, и этим самым дал способ получения этих очень интересных лабильных веществ. Вряд ли можно сомневаться, что этот метод найдет свое применение, в особенности в области физиологически действующих веществ при помощи коротких волн ультра-фиолетовых лучей. Далее, удалось получить таким путем эфиры из органических кислот, из спиртов, и естественно предположение, что эфиры, так часто встречающиеся в растительном мире, обязаны этому фактору (ведь солнечный свет также содержит ультра-фиолетовые лучи) своим образованием.
"Микронизирование" нашло применение и при другом важном физическом факте — давлении. Уже давно было известно применение низкого давления: при очистке веществ, высушивании, перегонке, сублимации долгое время пользовались аппаратурой Бунзена, состоявшей из водяного насоса, дававшего давление в 10—15 мм. ртути, насосы масленые и ртутные с дробными долями мм. ртути были очень дороги и поэтому лишь редко применялись. Конструированный Volmer’ом и Friedrich’ом аппарат быстро входит в общее применение, и за последнее время изолировано много соединений, как, например, фитол, составляющий часть хлорофилла, что вряд ли было бы возможно без применения весьма низкого давления. Непосредственные химические реакции при низком давлении еще незначительны, но мы можем уже указать на опыты Harries и Staudinger расщепления терпеновых углеводородов на молекулы изопрена, который может при помощи термического распада образоваться из каучука и обратно полимеризуется в каучук.
Подобно неорганической химии, в органической химии большую роль играют катализаторы и ферменты. В этой области в новейшее время достигнуты большие успехи, в особенности в области каталитического гидрирования. Сабатье открыл, что небольшое количество тонко распыленного никкеля, если он соприкасается с парами органических веществ, реагирующих с водородом, ускоряет реакцию, Paal Skita и Willstätter нашли, что никкель может быть заменен другим металлом (Pt и Pd), акад. В. Н. Ипатьев показал, что повышение давления водорода делает возможным гидрирование. В последнее время бесконечное число соединений было гидрировано, и во многих случаях этот метод оказался чрезвычайно важным для практики (гидрирование жиров и нафталина), ненасыщенные жидкие жиры превращаются в имеющие большую ценность твердые жиры и, наоборот, твердый нафталин, присоединяя 4 атома водорода, переходит в жидкий тетрагидронафтол (тетранилин), присоединяя 10 атомов водорода, — в жидкий декагидронафталин (декалин); оба имеют большое значение, как суррогаты бензина в моторах и для замены терпентина в лаковой промышленности (V. Gwinner, Schrauth). Производные тетранилина имеют значение фармакологическое. Никкель и медь при изменении условий могут также вызывать обратный процесс дегидрирования, которое сводится к окислению, и невольно возникает вопрос: нельзя ли было бы и молекулярный кислород при помощи катализаторов заставить реагировать с органическими веществами.
Значение катализаторов в биологических процессах имеет особое значение и работы в этой области только начинаются. Пионером является мюнхенский органик Вильштеттер, и эти исследования, как и все указанные выше достижения в области органо-химического анализа (в широком смысле этого слова), ясно показывают стремление органической химии использовать достижения физики и кристаллографии с одной стороны и биологические методы, — с другой.
(Более подробное изложение новых методов работ в области органической химии см. J. у. Braun, Z. f. angew. Ch. 1922, 2)
М. А. Блох.